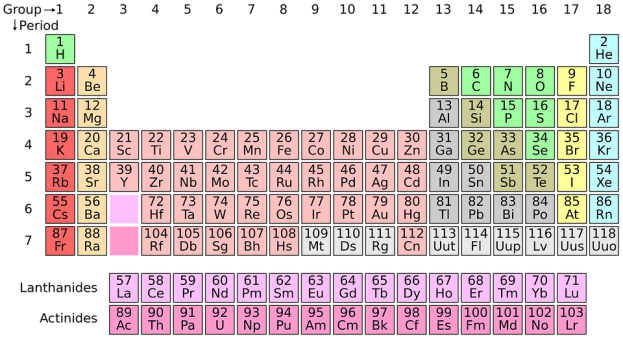
Atomens inre – Du kan lära dig om atomens inre och struktur under ” Lektioner om atomer och molekyler.
Länkar till sidor om atomens inre
Lektioner om om atomer och molekyler.
Lektion 2 – Kolla dina kunskaper
Strålning
Vi utsätts för olika typer av strålning i vår vardag. En del av denna strålning är inte bra för oss medan andra hjälper oss.. Ljus är till exempel en typ av elektromagnetisk strålning som är en förutsättning för att livet ska kunna existera på vår planet. Vi får ljus från vår närmaste stjärna solen som skickar hit ljus med olika våglängder. En del mer energirika än andra. Ultraviolett ljus är det mest energirika ljuset som vi får från solen. Det är det som gör att vi får röd hud när vi solar oss på sommaren om vi inte skyddar oss. Det synliga ljuset som solen skickar ut är inte lika energirikt och skadar oss inte på samma sätt.
En annan typ av strålning som vi stöter på är röntgenstrålning. Varje gång vi går till tandläkaren blir våra tänder röntgade för att tandläkaren ska se om det finns något som inte är bra och som hen inte ser med hjälp av den vanliga undersökningen. Vi får också röntga oss om man misstänker att vi till exempel har brutit ett ben. Röntgentrålningen är ännu mer energirik än vad det ultravioletta ljuset är. Med röntgenstrålning kan man se igenom hud och muskler. Fett, muskler, ben och annan vävnad fångar upp strålningen olika mycket. Ben i form av skelettet absorberar strålningen mest och blir därför ljusast på röntgenbilden.
Det finns också alltid en liten bakgrundstrålning,( naturlig radioaktivitet), i vår omgivning. Den kommer från tre olika källor. Kosmisk trålning från rymden, gammastrålning från radioaktiva ämnen i marken och från radioaktiva isotoper som finns i vår egen kropp.
Hur skapas ljus?
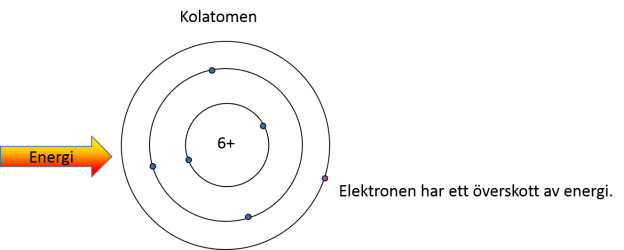
Om man förenklar verkligheten så är det så att atomernas elektroner är ordnade i olika skal. Elektronerna har olika energi beroende på i vilket skal de befinner sig i. När atomen tillförs energi så kan en elektron hoppa från ett inre till ett yttre skal. Elektronen får då överskottsenergi som den behöver göra sig av med eftersom det är ett tillstånd som atomen inte kan befinna sig i någon längre stund.

Presentation strålning-ljus
Alfastrålning
Alfastrålning består av partiklar nämligen en heliumkärna. Det vill säga en två protoner och två neutroner. Det är en positivt laddad partikel eftersom den inte innehåller några elektroner utan bara består av en heliumkärna. När heliumpartikeln lämnar atomkärnan så minskat atomnumret med 2. Det bildas ett nytt ämne som eftersom att antalet protoner har ändrats dvs minskat med 2.

Radium är ett radioaktivt ämne som avger alfastrålning. Radium har 88 protoner och den vanligaste isotopen har atommassan 226. När Radium skickar ut en alfapartikel, ( heliumkärna), så minskar atomnumret med 2 till 86 vilket är radon som också är ett radioaktivt ämne. Atommassan minskar med 4 till 222.
Alfastrålning har en kort räckvidd. Den når bara några centimeter i luft. Alfastrålningen stoppas också lätt utav olika material. Den stoppas av ett papper, kläder och av vår hud. Alfastrålning som kommer utifrån vår kropp är inte farlig för oss eftersom det så lätt stoppas. Däremot kan sådan strålning som av någon anledning kommer in i kroppen . Ett exempel kan vara radon. Radon kan finnas i marken under våra hus och därigenom komma in med luften. Att andas in luft som innehåller radon kan göra att vi får till exempel lungcancer. Det är därför viktigt att våra bostäder ventileras på ett korrekt sätt.
Betastrålning
Betastrålning består också av partiklar men mycket mindre partiklar än vad alfastrålning gör. Betastrålning består av elektroner. Så betastrålning är alltså negativt laddade partiklar eftersom att elektroner är negativt laddad. Det speciella med detta är att det är kärnan som skickar ut en negativ partikel men atomkärnan innehåller ju bara positiva partiklar. Det som sker är att en neutron omvandlas till en proton plus en elektron och elektronen lämnar kärnan medan protonen blir kvar i atomkärnan och ett nytt ämne har bildats. När ett radioaktiv ämne lämnar ifrån sig en betapartikel så kommer antalet protoner att öka med en medan antalet neutroner minskar med en.

Kol-14 är ett radioaktivt ämne som sänder ut strålningen i form av betapartiklar. När en av kolets 14 neutroner omvandlas till en proton samt en elektron så ökar antalet protoner från 6 till 7 och antalet neutroner minskar från 8 till 7.Atommassan ändras däremot inte eftersom att protonen och neutronen har samma massa.
Betastrålningen når längre än vad alfastrålningen gör. Betapartiklen ha en räckvidd på på ett par meter. Den kan också ta sig genom mer material än vad alfapartikeln kan göra vilket gör betastrålningen farligare. Betapartikeln når någon centimeter in i levande vävnad. Den stoppas också av en plexiglasskiva som är någon centimeter eller ett tjockt lager kläder.
Animering alfa och beta-strålning
Animering – alfa och beta-sönderfall
Gammastrålning
Gammastrålning består inte av någon partikel utan är elektromagnsetisk strålning av samma typ som ljus men med mycket mer energi. Gammastrålning når ett par hundratal meter i luft. Den tränger igenom det mesta och stoppas bara i princip helt av bly, I betong och sten kan den nå några meter. Det är därför svårt att skydda levande organismer mot gammastrålning.Precis som infrarött och ultraviolett ljus samt röntgenstrålning så kan man inte se gammastrålningen. Gammastrålning brukar sändas ut samtidigt som en atomkärna sänder ut alfastrålning och betastrålning. Eftersom att gammastrålning är elektromagnetisk strålning så påverkas varken atomnumret eller atommassan när den sänds ut. Den är ingen partikel och har därmed inte heller någon massa.
Röntgenstrålning
Röntgenstrålning har fått sitt namn av sin upptäckare Alfred Röntgen. Röntgenstrålning är en typ av elektromagnetisk strålning som uppkommer när en elektron i ett av de innersta skalen slås ut och ersätts av en elektron från ett yttre skal. Det vill säga att när det bildas röntgenstrålning så sker det på liknande sätt som när det bildas ljus.Röntgentrålningen är mycket energirik. Med röntgenstrålning kan man se igenom hud och muskler. Fett, muskler, ben och annan vävnad fångar upp strålningen olika mycket. Ben i form av skelettet absorberar strålningen mest och blir därför ljusast på röntgenbilden.
Film: Radioaktivitet och strålning – Obs kräver inloggning på SLI.se
Kort film på engelska om röntgenstrålning
Så här kan man stoppa strålning
Halveringstid
I ett radioaktivt ämne så faller inte atomkärnorna sönder samtidigt utan det sker efterhand. Det är väldigt olika med vilken snabbhet det här sker. Man anger hur snabbt det sker med halveringstid. Med halveringstid så menas tiden det tar för en radioaktivt ämne att sönderfalla så att hälften av atomkärnorna fallit sönder och bildat ett nytt ämne medan hälften av det ursprungliga radioaktiva ämnet finns kvar.
Halveringstiden är mycket olika för för olika radioaktiva ämnen. Det varierar från bråkdelen av en sekund till miljarder år.
Ett radioaktivt ämnes halveringstid är den tid det tar innan ämnets ursprungliga radioaktiva aktivitet har gått ner till hälften.
Kol – 14 är ett radioaktivt ämne som alla levande organismer får i sig så länge de lever. Det gäller för både växter och djur. Så länge organismen lever så är mängden kol- 14 konstant. När organismen dör så tillförs inte längre något kol – 14. Eftersom ett kkol – 14 är radioaktivt kommer de att falla sönder. Eftersom att kol – 14 har halveringstiden 5600 år så finns bara hälften av mängden kvar efter 5600 år. Efter ytterligare 5600 år så finns bara en fjärdedel kvar och efter ytterligare 5600 år så finns endast 1/8 kvar. På detta sätt fortsätter. Det är därför man kan åldersbestämma gamla döda träd, benknotor mm med kol -14-metoden.
Några halveringstider:
- Uran-238, 4,5 miljarder år
- Kol-14, 5 730 år
- Plutonium-239, 24 000 år
- Cesium-137, 30 år
- Radon-222, 3,8 dygn
- Jod -131, 8,1 dygn
- Xenon – 133, 5,24 dygn
Bequerel
Enheten för sönderfall heter bequerel ( Bq) efter den franske fysikern Henri Bequerel. 1 bequerel är ett sönderfall på en sekund. I och med att Bq är en enhet för antalet sönderfall per sekund för en avgränsad mängd radioaktivt ämne så beror aktiviteten både av hur intensivt ämnet sönderfaller samt storleken på den avgränsade mängden.
Film – radioaktivitet obs! Kräver inloggning på SLI
Källa: http://www.stralsakerhetsmyndigheten.se/Om-myndigheten/Aktuellt—Bilagor/Forklaring-av-begrepp/